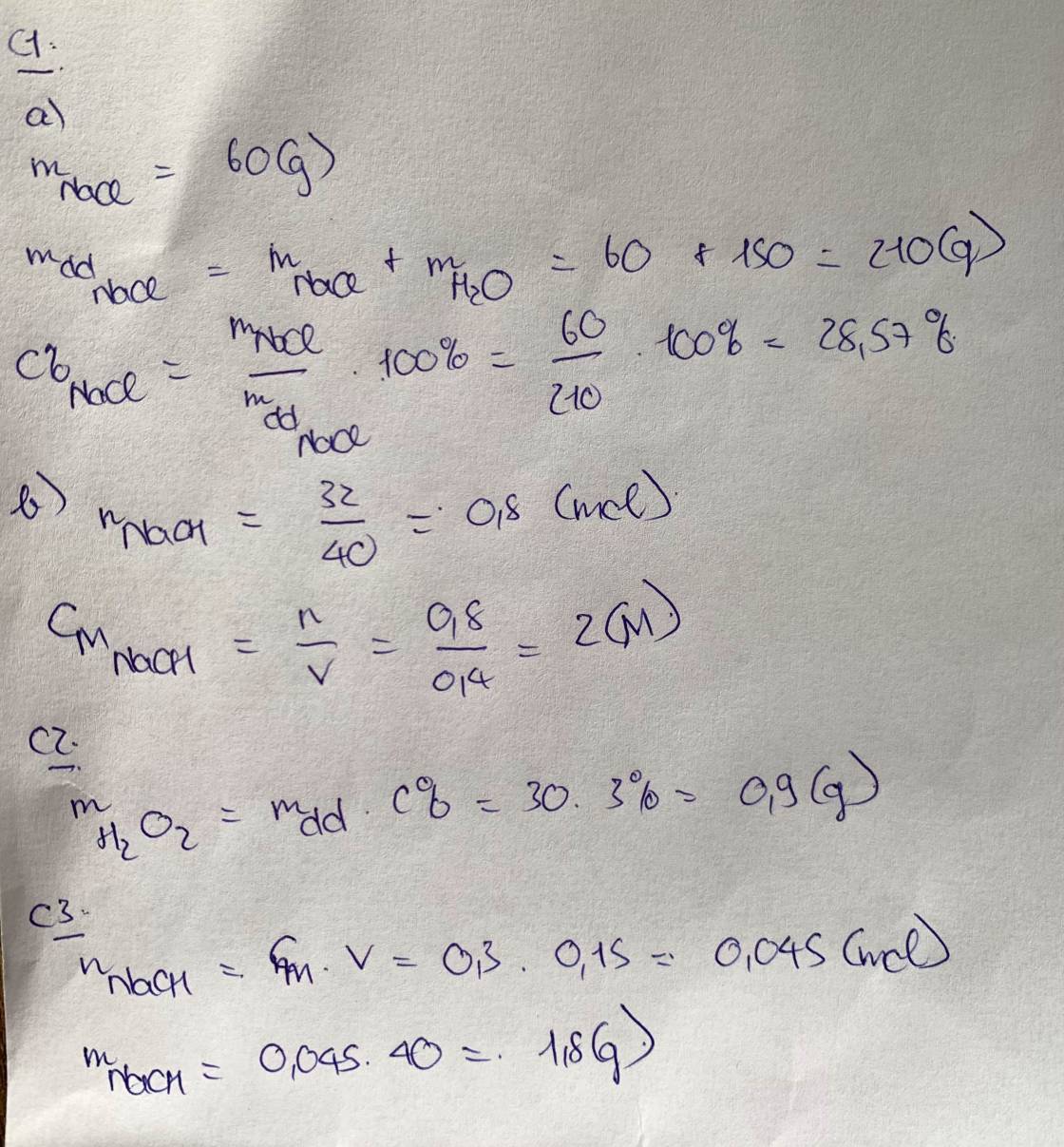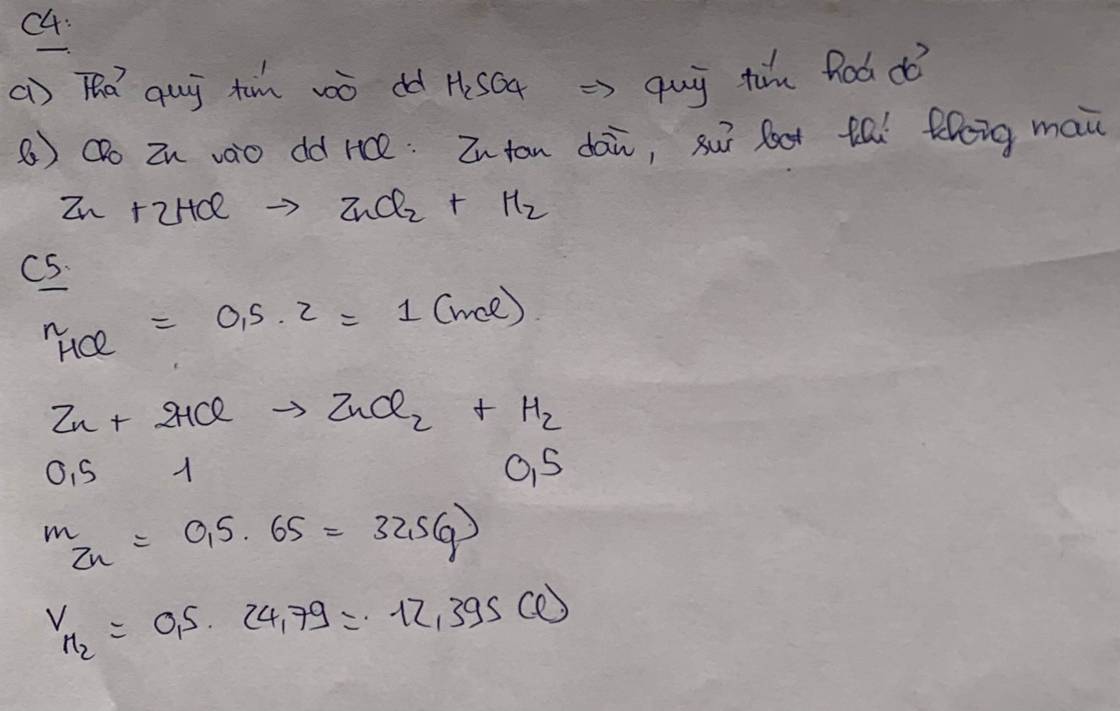Bài 7: hoà tan 21,6 g NaOH vào 400 gam nước được dung dịch A
a. tính khối lượng dung dịch A
b.tính thể tích tích dung dịch A
c) tính nồng độ mol/lit nồng độ phần trăm của cac chất trong dung dịch A
MN giải chi tiết và đơn giản giúp mình vs

Những câu hỏi liên quan
Câu 8: Cho 99,4 gam P2O5 vào 500 gam nước (dư), thu được dung dịch A.
a. Tính khối lượng chất tan, khối lượng nước trong dung dịch A.
b. Tính nồng độ phần trăm dung dịch A.
c. Tính nồng độ mol/l của dung dịch A. Biết thể tích dung dịch A là 500 ml.
giúp vs ae
\(n_{P_2O_5}=\dfrac{99,4}{142}=0,7\left(mol\right)\)
\(P_2O_5+3H_2O\rightarrow2H_3PO_4\)
0,7 2,1 1,4
a, \(m_{H_3PO_4}=1,4.98=137,2\left(g\right)\)
\(m_{ddH_3PO_4}=99,4+500=599,4\left(g\right)\)
Kl nước trong dd A :
\(m_{H_2O}=599,4-137,2=462,2\left(g\right)\)
\(b,C\%_{H_3PO_4}=\dfrac{137,2}{599,4}.100\%\approx22,89\%\)
\(c,C_M=\dfrac{n}{V}=\dfrac{1,4}{0,5}=2,8M\)
Đúng 2
Bình luận (0)
Hoà tan 50 gam đường vào nước thu được 400 gam dung dịch đường. Biết nồng độ phần trăm của dung dịch này là tỉ số phần trăm của khối lượng đường trong dung dịch sau khi hoà tan. Tính nồng độ phần trăm của dung dịch đường
Em đăng vào môn Hoá hấy
Đúng 0
Bình luận (0)
Câu 1 a. Hòa tan 60 gam NaCl vào 150 gam nước. Tính nồng độ phần trăm của dung dịch thu được.b.Tính nồng độ mol của dung dịch khi hòa tan 32 gam NaOH trong 400ml nước. (coi thể tích dung dịch không đổi).Câu 2 Hãy tính khối lượng H2O2 có trong 30 g dung dịch nồng 3% .Câu 3 Tính khối lượng của NaOH có trong 300 ml dung dịch có nồng độ 0,15 M.Cho Na 23; O 16; H1.Câu 4Hãy nêu , giải thích được hiện tượng xảy ra trong thí nghiệm và viết phương trình hoá học .Từ đó rút ra nhận xét về tính chất...
Đọc tiếp
Câu 1
a. Hòa tan 60 gam NaCl vào 150 gam nước. Tính nồng độ phần trăm của dung dịch thu được.
b.Tính nồng độ mol của dung dịch khi hòa tan 32 gam NaOH trong 400ml nước. (coi thể tích dung dịch không đổi).
Câu 2 Hãy tính khối lượng H2O2 có trong 30 g dung dịch nồng 3% .
Câu 3 Tính khối lượng của NaOH có trong 300 ml dung dịch có nồng độ 0,15 M.
Cho Na= 23; O= 16; H=1.
Câu 4
Hãy nêu , giải thích được hiện tượng xảy ra trong thí nghiệm và viết phương trình hoá học .Từ đó rút ra nhận xét về tính chất của acid khi thực hiện các thí nghiệm sau:
a.Thả miếng giấy quì tím vào lọ đựng dung dịch sulfuric acid (H2SO4)
b.Cho viên kẽm (zinc) vào trong ống nghiệm có chứa dung dịch hydrochloric acid.
Câu 5
Cho kẽm (Zinc) dư tác dụng với 500 ml dung dịch hydrochloric acid 2 M, thu được V (lít) khí hydrogen (250C và 1 bar).
Tính khối lượng kẽm đã phản ứng và thể tích khí hydrogen thu được.
Hoà tan 50 gam đường vào nước thu được 400 gam dung dịch đường. Biết nồng độ phần trăm của dung dịch này là tỉ số phần trăm của khối lượng đường trong dung dịch sau khi hoà tan. Tính nồng độ phần trăm của dung dịch đường
Giải hộ mình nếu còn thức :(((
a,tính khối lượng NaOH có trong 200ml dung dịch NaOh 1M b,tính số mol H2SO4 có trong 100ml dung dịch H2SO4 2M c,hoà tan 6g NaCl vào nước thu được 200g dung dịch tính nồng độ phần trăm của dung dịch d,tính khối lượng NaCl có trong 200g dung dịch NaCl 8%
a, \(n_{NaOH}=0,2.1=0,2\left(mol\right)\)
\(m_{NaOH}=0,2.40=8\left(g\right)\)
b, \(n_{H_2SO_4}=2.0,1=0,2\left(mol\right)\)
\(c,C\%=\dfrac{6}{200}.100\%=3\%\)
\(m_{NaCl}=\dfrac{200.8}{100}=16\left(g\right)\)
Đúng 1
Bình luận (0)
bài 2 :hoà tan 10g đường vào 100g nước được dung dịch nước đường . Tính nồng độ phần trăm của dung dịch nước đường thu được
bài3: hoà tan 4g NaOH vào nước được 200ml dung dịch . Tính nồng đọ mol của dung dịch thu được
Bài 2
\(C_{\%đường}=\dfrac{10}{10+100}\cdot100\%\approx9,09\%\)
Bài 3
\(n_{NaOH}=\dfrac{4}{40}=0,1mol\\ C_{M_{NaOH}}=\dfrac{0,1}{0,2}=0,5M\)
Đúng 1
Bình luận (0)
1. Hoà tan 6,2 g natri oxit vào 193,8 g nước thì được dung dịch A. Tính nồng độ phần trăm của dung dịch A.2. Hoà tan 23,5 g kali oxit vào nước được 0,5 lít dung dịch A. Tính nồng độ mol của dung dịch A.3. Hòa tan hết 12,4 gam natrioxit vào nước thu được 500ml dung dịch A . Tính nồng độ mol của dung dịch A.4. Hòa tan 12,6 gam natri sunfit vào dung dịch axit clohidric dư. Thể tích khí SO2 thu được ở đktc.5. Hòa tan hết 5,6 gam CaO vào dung dịch HCl 14,6% . Tính khối lượng dung...
Đọc tiếp
1. Hoà tan 6,2 g natri oxit vào 193,8 g nước thì được dung dịch A. Tính nồng độ phần trăm của dung dịch A.
2. Hoà tan 23,5 g kali oxit vào nước được 0,5 lít dung dịch A. Tính nồng độ mol của dung dịch A.
3. Hòa tan hết 12,4 gam natrioxit vào nước thu được 500ml dung dịch A . Tính nồng độ mol của dung dịch A.
4. Hòa tan 12,6 gam natri sunfit vào dung dịch axit clohidric dư. Thể tích khí SO2 thu được ở đktc.
5. Hòa tan hết 5,6 gam CaO vào dung dịch HCl 14,6% . Tính khối lượng dung dịch HCl đã dùng.
Cho em xin cách giải chi tiết ạ em cảm ơn :DD
1)
$n_{Na_2O} = \dfrac{6,2}{62} = 0,1(mol)$
$Na_2O + H_2O \to 2NaOH$
$n_{NaOH} = 2n_{Na_2O} = 0,2(mol)$
$m_{dd} = 6,2 + 193,8 = 200(gam) \Rightarrow C\%_{NaOH} = \dfrac{0,2.40}{200}.100\% = 4\%$
2)
$n_{K_2O} = \dfrac{23,5}{94} = 0,25(mol)$
$K_2O + H_2O \to 2KOH$
$n_{KOH} = 2n_{K_2O} = 0,5(mol) \Rightarrow C_{M_{KOH}} = \dfrac{0,5}{0,5} = 1M$
3) $n_{Na_2O} = \dfrac{12,4}{62} = 0,2(mol)$
$Na_2O + H_2O \to 2NaOH$
$n_{NaOH} = 2n_{Na_2O} = 0,4(mol)$
$C_{M_{NaOH}} = \dfrac{0,4}{0,5} =0,8M$
Đúng 3
Bình luận (1)
4)
$Na_2SO_3 + 2HCl \to 2NaCl +S O_2 + H_2O$
Theo PTHH :
$n_{SO_2} = n_{Na_2SO_3} = \dfrac{12,6}{126} = 0,1(mol)$
$V_{SO_2} = 0,1.22,4 = 2,24(lít)$
5) $n_{CaO} = \dfrac{5,6}{56} = 0,1(mol)$
$CaO + 2HCl \to CaCl_2 + H_2O$
Theo PTHH :
$n_{HCl} = 2n_{CaO} = 0,2(mol) \Rightarrow m_{dd\ HCl} = \dfrac{0,2.36,5}{14,6\%} = 50(gam)$
Đúng 3
Bình luận (1)
Bài 1 :
\(n_{Na2O}=\dfrac{6,2}{62}=0,1\left(mol\right)\)
Pt : \(Na_2O+H_2O\rightarrow2NaOH|\)
1 1 2
0,1 0,2
\(n_{NaOH}=\dfrac{0,1.2}{1}=0,2\left(mol\right)\)
⇒ \(m_{NaOH}=0,2.40=8\left(g\right)\)
\(m_{ddspu}=6,2+193,8=200\left(g\right)\)
\(C_{ddNaOH}=\dfrac{8.100}{200}=4\)0/0
Chúc bạn học tốt
Đúng 2
Bình luận (1)
Xem thêm câu trả lời
Hòa tan hoàn toàn 3,1 g Na2O vào 500ml nước thu được dung dịch A
a- Viết PTHH cho biết dd A làm quỳ tím đổi màu như thế nào ?
b- Tính nồng độ mol của dung dịch A (Xem như thể tích dung dịch không đổi)
c- Tính khối lượng dung dịch A
d- Tính nồng độ phần trăm của dung dịch A (Biết khối lượng riêng của nước là 1 g/ml)
a, \(n_{Na_2O}=\dfrac{3,1}{62}=0,05\left(mol\right)\)
PTHH: Na2O + H2O → 2NaOH
Mol: 0,05 0,1
⇒ ddA (NaOH) làm quỳ tím đổi màu xanh
b, \(C_{M_{ddNaOH}}=\dfrac{0,1}{0,5}=0,2M\)
c, \(m_{ddA}=3,1+1.500=503,1\left(g\right)\)
d, \(C\%_{ddNaOH}=\dfrac{0,2.40.100\%}{503,1}=1,59\%\)
Đúng 2
Bình luận (0)
Hoà tan V lit HCl (đktc) vào 192,7 ml nước thì thu được dung dịch HCl 3,65%
a/ Tính V
b/ Tính nồng độ mol của dung dịch. Suy ra khối lượng riêng của dung dịch. Sự hoà tan không làm thay đổi thể tích chất lỏng
192,7 ml = 0,1927 lít
192,7 ml = 192,7 g
Ta có
C% = mct / mdd x 100%
=> m ct = C% x mdd / 100% = 3,65% x 192,7 / 100% = 7,03355 gam
n HCl = mct / M HCl = 7,03355 / 36,5 = 0,1927 mol
Ta lại có :
CM = (10*D*C%)/M
CM = (10*1.18*3.65) / 36.5 ≈ 1.18 M
D HCl = 1.18
Đúng 0
Bình luận (1)